2020年6月29日に「化粧品監督管理条例」の公布に伴い、国家薬品監督管理局(NMPA)は7月21日に「化粧品登録管理弁法(意見募集稿)」(下記は同弁法という)を発表し、社会各界から意見を求め始めるようになりました。公衆は、次のルート及び方式を通じで意見やフィードバックを提出することができます。
1. 中華人民共和国司法部中国政府法制情報網(URL:www.moj.gov.cn、www.chinalaw.gov.cn)のトップページのメインメニューの「立法意見募集」欄に意見を提出することは可能です。
2. 書面という形で郵送することは可能です。住所:北京市西城区展覧路北露園1号、郵便番号:100037。そして封筒に「化粧品登録管理方法意見募集」と書いておいてください。
3. 電子メールという形です。電子メールアドレス:huazhuangpinchu@163.com。
意見募集の締切日は、2020年8月20日までです。
当社では、同弁法及び同弁法における化粧品新原料に関する内容を下記の通りにまとめさせていただきます。
同弁法は全部で7章88条で、総則、基本要求、化粧品新原料登録・届出管理、化粧品登録・届出管理、監督管理、法律責任、附則からなります。
第1章:総則(第1~7条) |
内容:制定根拠、適用範囲、定義、分類管理、国家薬品監督管理局職権、省級薬品監督管理局職権、情報公開 |
主な内容: (1)登録と届出の定義
(2)化粧品種類によって分類管理
(3)当局の各部門の職責の明確化
|
第2章:基本要求(第8~13条) |
内容:登録者、届出者に関する定義、責任、要求、国内責任者の義務を明確にしました。専門家のコンサルティングメカニズムを追加しました。 |
|
第3章は化粧品の新原料には登録・届出管理及び安全検査と報告の要求も含み、主に事前登録の審査段階の流れと所要時間についての規定です。その中には、事後監督管理は以前よりもっと細かく明確化されたことがわかりました。当社では、各種類の化粧品新原料の登録・届出申請の流れを下記の通りにまとめさせていただきます。
- 輸入化粧品新原料の届出
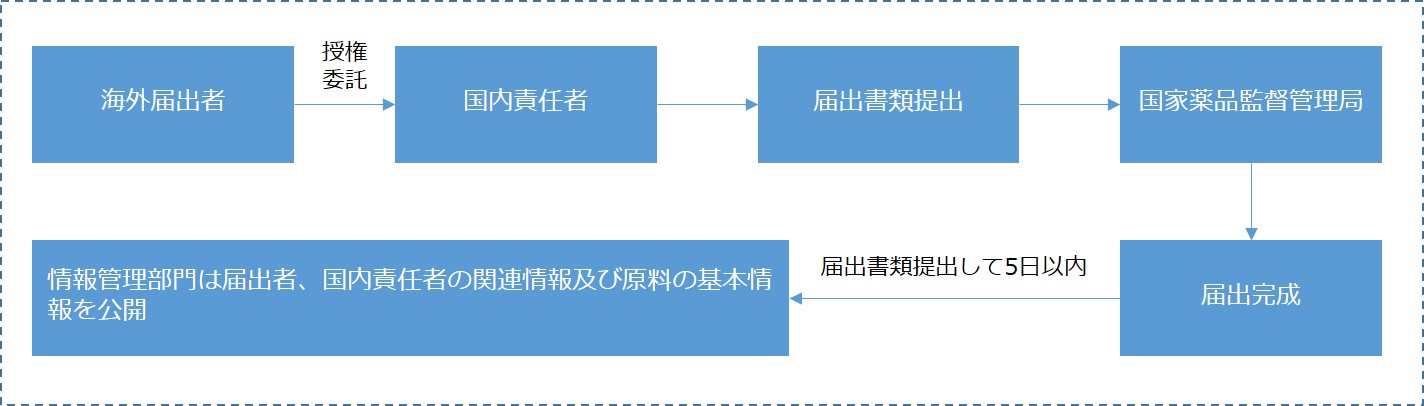
- 国産化粧品新原料届出
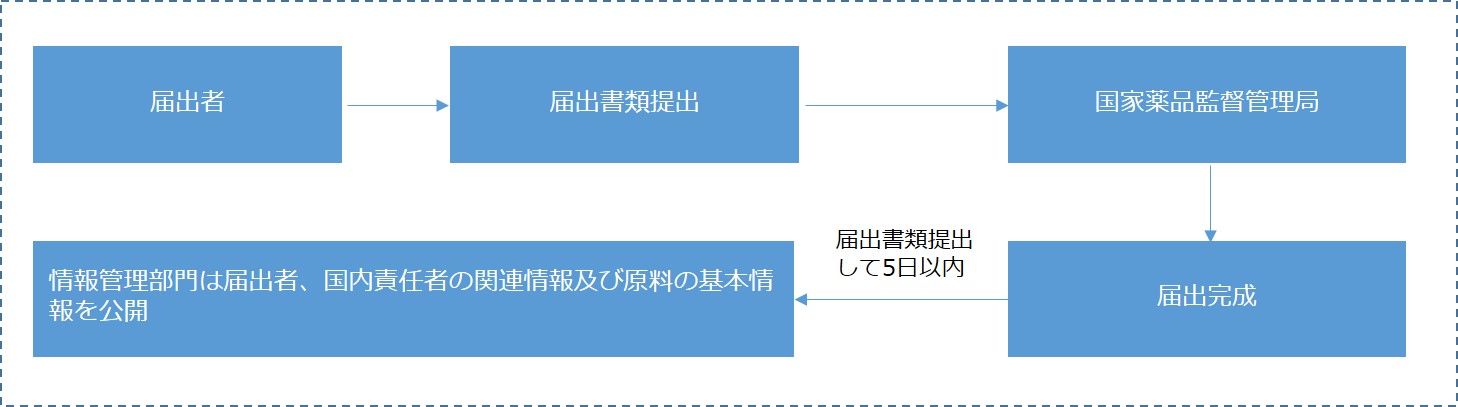
- 輸入化粧品新原料登録
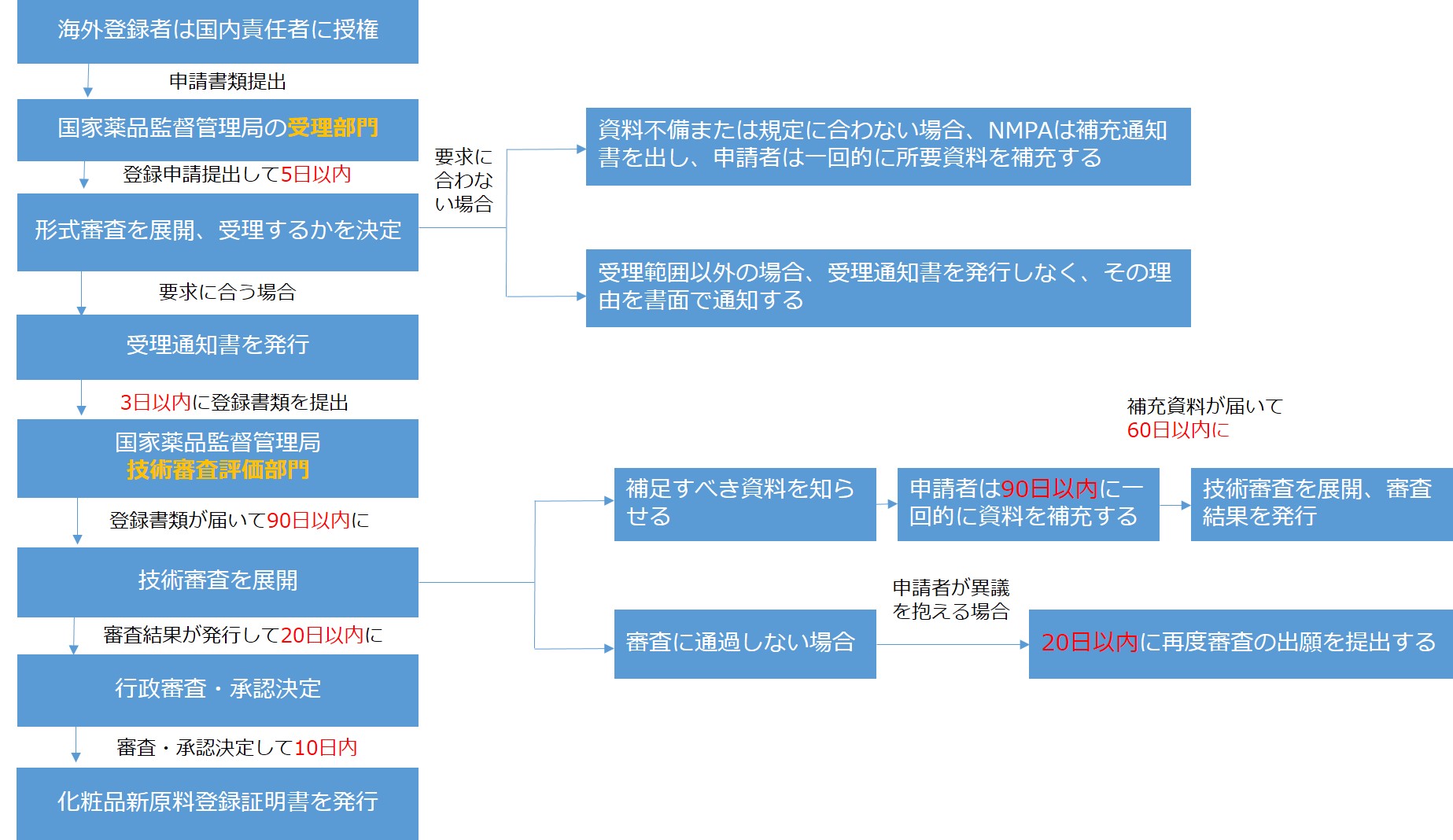
- 国産化粧品新原料登録

NMPAは登録・届出済みの新原料に対して安全モニタリングを行うことになります。初めて化粧品に新原料を使用する場合は、登録・届出済みの日から3年の安全モニタリング期間を設定するようになります。登録・届出済みの新原料の使用方法とモニタリングの詳細は下記の通りです。
- 安全モニタリングの3年期間以内の場合
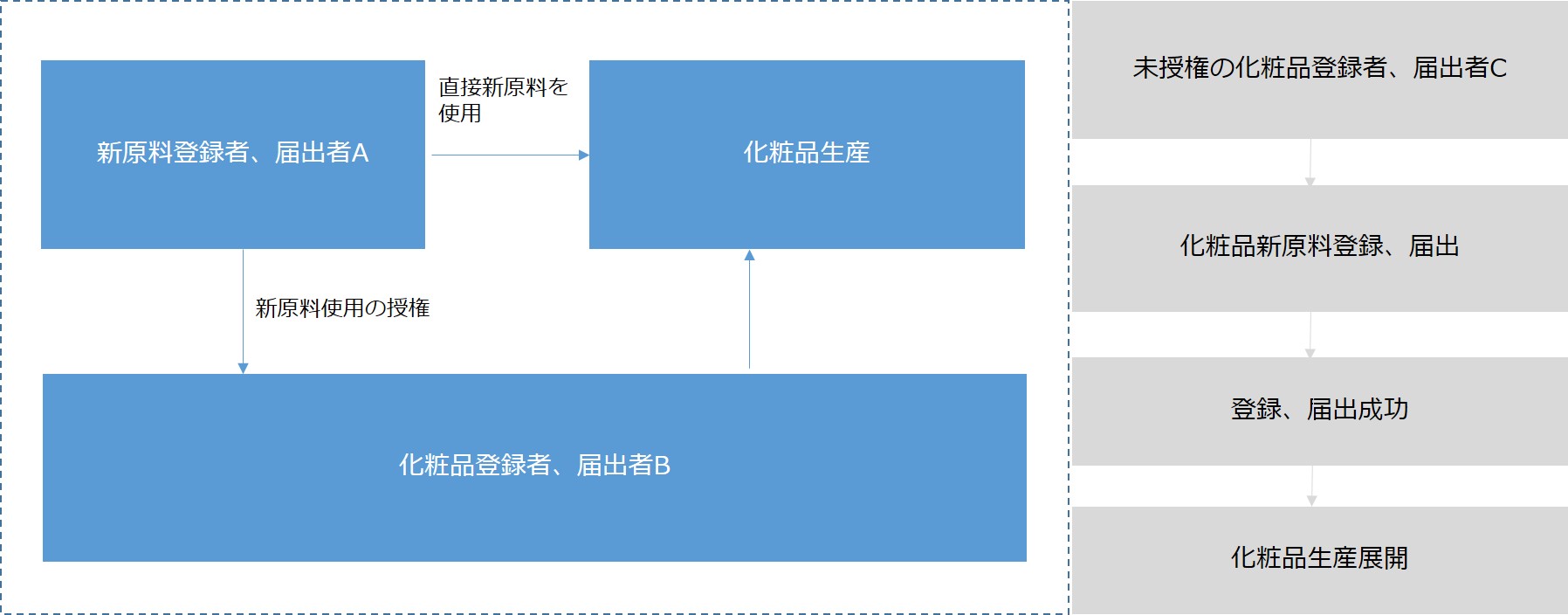
- 安全モニタリングの3年期間が満了の場合

- 登録・届出済みの新原料に対するモニタリング
新原料の登録者、届出者、及び新原料を使用して化粧品を生産する登録者、届出者はモニタリングに関する責任を履行すべきです。責任の詳細は下記のとおりです。
監督責任 新原料登録者、届出者 新原料を使用する登録者、届出者 新原料の発売後の安全リスク監視と評価システムを確立し、新原料の使用の安全状況を持続的に注目し、研究、モニタリングと評価を行う必要がある。 新原料使用の安全状況をリアルタイムで監視し、新原料登録者、届出者に新原料の使用状況、関連化粧品の不良反応と安全性状況を報告する必要がある。
新原料を使って化粧品を生産する登録者、届出者 | 製品状況報告 |
| |
新原料登録者、届出者 | 原料状況報告 |
| |
年度報告 | 新原料への安全監視は1年ごとに、新原料の使用状況と安全状況に関するまとめ、その分析を年度報告書に不良反応監視部門と技術審査部門に報告する。 | ||
省、自治区、直轄市薬品監督管理部門 | 製品報告対応 |
|
国家薬品監督管理局技術審査部門 | 安全報告対応 |
|
不良反応監視部門 | 年度報告対応 | 年度報告に合わせて、新原料化粧品に関する不良反応をまとめ、報告書を作成する。 |
国家薬品監督管理局技術審査部門 |
|
- まとめ
♢ 同弁法によると、核心内容となる化粧品、新原料の登録・届出に関わる行政制度、関連者の責任と義務を明確にしたことが分かりました。主な内容は下記の通りにまとめさせていただきます。
♢ 業界の要望に応えて、審査を無断に長引くことを避けるために補足回数、期限を明確にして、審査承認の異動を防ぐために登録資料を提出した途端に登録済みになることと決めました。
♢ 同弁法は党中央国務院の「緩和・管理・サービス」改革の方針に基づいたものとして、リスクが低い新原料に対して届出管理を行うことで、新原料の市場参入の効率を高めることを狙っています。
♢ 登録・届出済みの新原料へのモニタリングを重点に当てています。新原料の登録者、届出者は新原料の使用中の安全状況という年度報告を毎年不良反応監視部門と技術審査部門に提出すべきです。不良反応や、安全性問題が出た場合、登録者、届出者は同原料に対して再度評価を行い、その結果を提出する必要があります。
♢ 新原料開発企業の積極性を維持するために、安全モニタリング期間中に新原料を使用しようとする企業は、新原料登録者、届出者から同意を取得してもらう必要があります。
♢ 同弁法によると、化粧品生産向けの原料は、使用実績がある原料の使用目的に外れ、または安全用量を超える場合、新原料として登録・届出を行う必要になることがわかりました。安全性に及ばない場合は、安全モニタリング期間を設けないことになっています。ということは、これから使用実績がある原料リストに各原料の使用目的と安全用量が追加される見込みです。



