化粧品の定義
皮膚、毛髪、爪、口唇等の人体表面に塗布、散布又はその他の類似の方法により、清潔、保護、美化及び修飾を目的とした日用化学工業製品。
化粧品の分類
特殊化粧品及び普通(一般)化粧品
- 特殊化粧品:髪染め、パーマ、シミ取り、美白、日焼け止め(UV)、脱毛防止、新効能を宣伝する化粧品
- 普通(一般)化粧品:特殊化粧品以外の化粧品(一般的なスキンケア/ヘアケア、ボディケア、ネイルケア、脱毛、消臭、香水、メイクアップなどの製品)
注:育毛、バストアップ、ボディビル類の製品は化粧品には該当しません。
化粧品の中国上市要求
現在、越境ECルートで販売された化粧品は登録・備案を免除されているほか、その他のルートで販売された化粧品(一般的な美容石鹸を除く)は、中国国家薬品監督局管理局(NMPA)または地方薬品監督管理局を通じて化粧品の登録・備案を完了してから市販される必要があります。中国は特殊化粧品に対して登録管理を実行し、普通(一般)化粧品に対して備案管理を実行します。
化粧品登録者、備案者に対する要求
化粧品の登録者、備案者は化粧品の品質安全及び効能宣伝に対して責任を負います。次の条件が必要です。
- 法により設立された企業又はその他の組織。
- 登録申請、備案を行う製品に適した品質管理システムがあること。
- 化粧品の不良反応モニタリングと評価能力があること。
境内責任者の義務
境外化粧品登録者及び備案者は、中国国内の企業法人を指定して化粧品の登録及び備案を行い、化粧品の不良反応モニタリング及び製品リコールの実施に協力しなければなりません。境内責任者は、以下の義務を履行しなければなりません。
- 登録者、備案者の名義で、化粧品、化粧品新原料の登録、備案を行うこと。
- 登録者、備案者に協力して化粧品の不良反応モニタリング、化粧品新原料の安全モニタリングと報告作業を展開すること。
- 登録者、備案者に協力して化粧品、化粧品新原料の回収作業を実施すること。
- 登録者、備案者との協議に基づき、中国国内市場に投入される化粧品、化粧品新原料に対して相応の品質安全責任を負うこと。
- 薬品監督管理部門の監督検査作業に協力すること。
化粧品登録備案の流れ
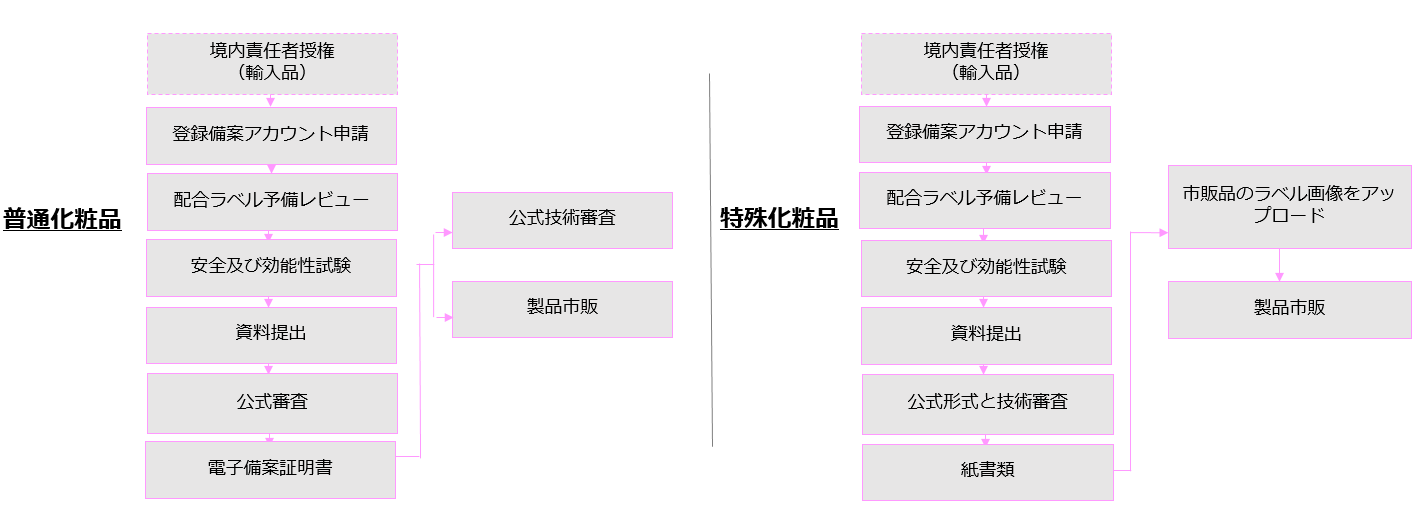
化粧品登録備案の資料要求
「化粧品登録備案管理規定」に基づき、化粧品登録備案申請には以下の資料を提出しなければなりません。
- 「化粧品登録備案情報表」及び関連資料
- 製品名情報
- 製品配合
- 製品実施基準
- 製品ラベルのドラフト
- 製品検査報告
- 製品安全性評価資料
化粧品の実験要求
登録又は備案製品の製品検査報告は、化粧品登録及び備案検査機構が発行するものであり、「化粧品安全技術規範」、「化粧品登録及び備案検査業務規範」等の関連法規の規定に合致しなければなりません。製品検査報告には次の内容が含まれます。
- 微生物実験
- 物理・化学実験
- 毒性実験
- 人体安全性試験(特殊化粧品適用)
- 人体効能試験報告書など
毒理学試験の実施を免除する条件:a)一般化粧品の生産企業が、所在国(地区)政府主管部門が発行した生産品質管理システム関連資格認証を取得します。b)かつ製品の安全リスク評価結果、製品の安全性を十分に確認できます。複数の生産企業が生産している場合、すべての生産企業が所在国(地区)政府主管部門が発行した生産品質管理体系の関連資格認証を取得している場合、毒性学試験報告の提出を免除することができます。
以下の条件に該当する場合、毒物実験は免除されません。
- 製品が乳幼児と子供の使用を宣伝している場合
- 製品はまだ安全モニタリング中の化粧品新原料を使用する場合
- 数量化等級評価の結果に基づき、備案者、境内責任者、生産企業が重点監督管理対象に指定された場合
化粧品ラベル要求
「化粧品ラベル管理弁法」により、化粧品の中国語ラベルには少なくとも以下の内容を含まなければなりません。
- 製品の中国語名称、特殊化粧品登録証明書番号
- 登録者、備案者の名称、住所、登録者又は備案者が境外企業である場合、同時に境内責任者の名称、住所を表記しなければならない
- 生産企業の名称、住所、中国国産化粧品は同時に生産企業の生産許可証番号を表記しなければならない
- 製品実行の標準番号
- 全成分
- 純含量
- 使用期間
- 使用方法
- 必要な安全警告用語
- 法律、行政法規及び強制性国家標準に表記すべき旨が規定されているその他の内容。
包装箱を有する製品は、同時に内容物に直接接触する包装容器に製品の中国語名称と使用期限を表記しなければなりません。
化粧品上市後の規制
普通(一般)化粧品:
- 主管部門は既に備案された化粧品の一部に対して技術審査を行います。
- 2022年からは、備案済みの化粧品は年次報告書を提出する必要があります。省級以上の人民政府の薬品監督管理部門は化粧品のサンプリング検査を行わなければなりません。申告又は日常の監督検査において問題が比較的多くと発見された化粧品に対し、薬品監督管理の主管部門は特別サンプリング検査を行うことができます。
CIRSの強み
- 化粧品業界の川上/川下企業にワンストップサービスを提供
- 製品の安全性とコンプライアンス
- 製品の迅速な市場投入
- 豊富な経験を持つ毒性学の専門家と法規チーム
- グローバルのパートナーシップ
- 厳格な秘密保持制度



