現行「中華人民共和国食品安全法」は、保健食品に対して厳格的な監督管理を行います。保健食品の管理を規範化、統一化させるために、中国国家市場監督管理総局(SAMR、元CFDA)は「保健食品登録及び届出管理弁法」、「保健食品登録申請服務指南」、「保健食品登録審査細則」などの法規制を制定し、保健食品の期限延長制度を確立し、期限延長申請する際の資料要求などを明確します。
「保健食品の期限延長」とは
保健食品の期限延長は、食品薬品監督管理部門が申請企業の申請に応じて、法定手続き、条件、要求などに基づき、保健食品許認可の有効期限を延長する申請を審査、認可することです。
保健食品期限延長を申請する際の資料要求
1. 国産保健食品
(1) 申請書及び法律責任承諾書
(2) 登録申請者主体登記証明資料のコピー件
(3) 保健食品許認可及びその付録のコピー件
(4) 省レベルの食品薬品監督管理部門が確かめた許認可有効期限内の製品製造販売状況(輸入保健食品の場合、書面の製品製造販売状況説明、国内代理店(或は輸入企業)が押印済み(或は法人署名済み)の経営許可書コピー件、貨物輸入通関書類とインボイスのコピー件を提出)
(5) 対象者食用状況の分析報告
(6) 製造品質管理体系の運行状況に対する自己検査報告
(7) 資格ある食品検査機構によって発行した許認可有効期限内の製品技術要求に合致する全項目検査報告(1ロット)
2. 輸入保健食品
国産製品の要求に従って上述した相関資料を提出する以外、以下資料を追加提出します。
(1) 製品製造国(地域)の政府主管機構又は法律サービス機構によって発行した証明書、申請者が保健食品の域外製造者であることを証明する
(2) 製品製造国(地域)の政府主管機構又は法律サービス機構によって発行した証明書、保健食品が1年以上の販売実績があることを証明する
(3) 製品製造国(地域)が製品に対して認可制度を執行する場合、製造国(地域)主管部門が製品販売を認可する証明書を提供する
(4) 製品製造国(地域)又は国際組織が公布した保健食品に関わる法規制(或は)標準原文
(5) 製品製造国(地域)に販売する製品の包装、ラベル、説明書の現物
(6) 域外申請者の中国国内拠点によって登録を申請する場合、「外国企業常駐中国代表機構登記証」のコピー件を提出する。域外申請者が中国国内の代理機構を委託して登録を申請する場合、公証された委託書の原本及び委託された代理機構の営業許可書のコピー件を提出する
保健食品期限延長を申請する際の注意事項
(1) 申請企業は保健食品許認可有効期限が切れる前(一般的に、有効期限が切れる前の6ヶ月以上)に保健食品期限延長を申請し、受理を取得すべきです。許認可有効期限が切れ、しかも、期限延長を申請していない場合、許認可は取り消されます。
(2) 製品原料が保健食品原料目録に収載され、しかも、相関技術要求に合致する場合、保健食品の「登録から届出へ変更」を申請しなければなりません。
(3) 期限延長を申請する製品の安全性、保健機能及び品質制御性は相関要求に合致しなければならなくて、許認可有効期限内に製造販売実績を有しなければなりません。
(4) 期限延長を申請する製品は2016年12月31日以前に既に変更、譲渡などの申請事項を申請して受理され、しかも、その審査認可はまだ進行中である場合、申請企業は前の申請事項が認可された後に30営業日以内に期限延長の申請を提出しなければなりません。
(5) 保健食品の原料種類、数量を変更してはいけません。
(6) 製品技術要求が現行法規制に合致する場合、その内容を変更してはいけません。現行法規制に合致しないため調整する必要な場合、現行法規制の要求に従って調整し、試験報告などの相関資料を追加提出しなけばなりません。
(7) 製品ラベル、説明書の設計は現行法規制に従って調整し、調整説明及び調整後のラベル、説明書設計を提出しなけばれなりません。
保健食品期限延長に関わる法規制
● 「中華人民共和国食品安全法」及びその実施条例
● 「保健食品登録及び届出管理弁法」
● 「保健食品登録申請服務指南」
● 「保健食品登録審査細則」
● 「保健食品再登録技術審査要点」
保健食品期限延長の流れ
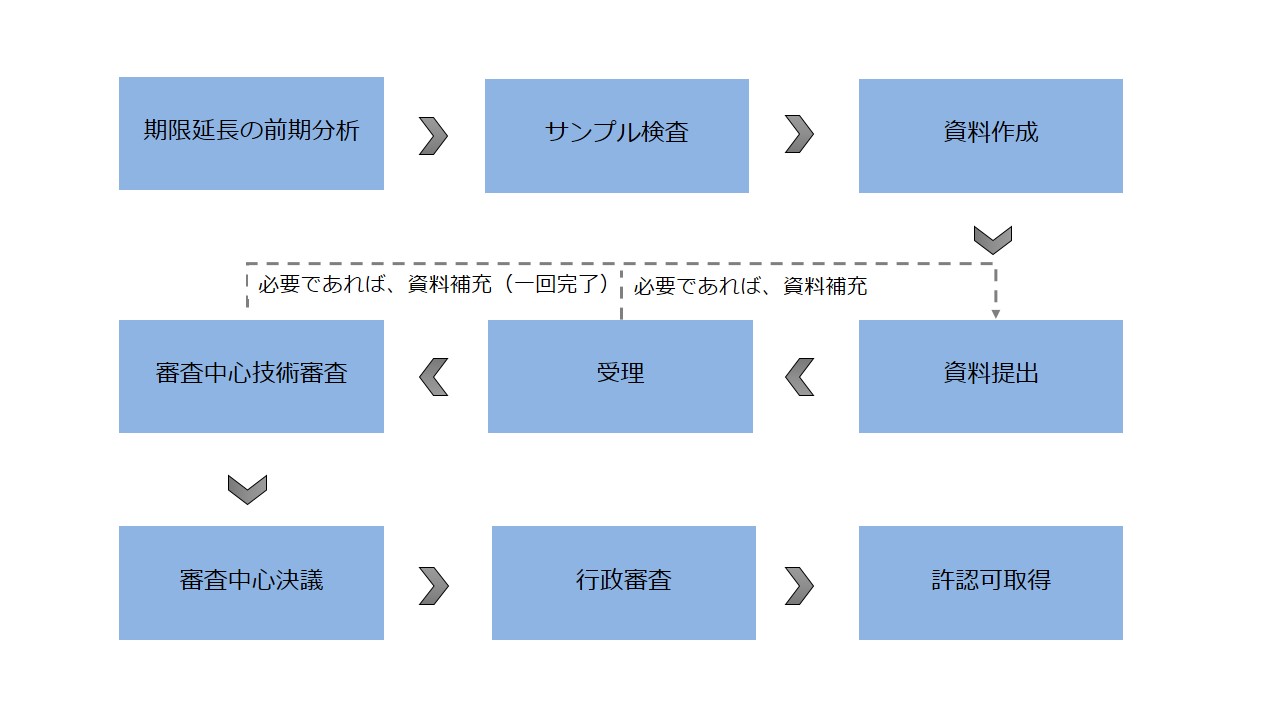
CIRSのザービス
CIRSはお客様に中国食品の法規制対応サービスを提供いたします。保健食品に対し、以下サービスを提供いたします。
• 保健食品の期限延長(再登録)
• 保健食品登録の代行
• 保健食品届出の代行
• 保健食品の登録変更
• 保健食品の法規トレーニング
• 保健食品の法規動向モニタリング
• 単項目技術サービス
√ 製品分類及び処方の実行性分析
√ 中国語ラベル及び包装説明書の設計
√ 書類準備
√ 翻訳
√ 試験手配及び進捗フォローアップ



