2019年以来、中国国家市場監督管理総局(SAMR)は健康食品登録及び届出双規制の進行を推進し、健康食品の管理要求を明確化するために、健康食品に関する政策法規を何回も公表しました。この度、これらの政策法規をまとめて紹介します。
2019年以来公表された関連した政策法規
項目 | 政策法規 | 施行/公表期日 |
正式バージョン | 「健康食品原料目録及び保健機能目録管理弁法」 | 2019.10.01から施行 |
2020.01.01から施行 | ||
意見募集稿 | 2019.03.20公表 | |
2019.04.01公表 | ||
2019.04.08公表 | ||
「健康食品用菌種致病性評価プロセス(意見募集稿)」 | 2019.04.08公表 | |
2019.06.04公表 | ||
「健康食品衛生学理化検験規範(意見募集稿)」 | 2019.06.19公表 | |
「特殊食品登録の現場審査規程(暫行)(意見募集稿)」 | 2019.07.17公表 |
健康食品届出製品の原料目録の拡大
2019年4月1日、中国国家市場監督管理総局はコエンザイムQ10、メラトニン、魚油、壊れた壁霊芝胞子パウダー及びスピルリナを含む5種類の原料を健康食品原料リストに追加する公告を公布し、社会意見の募集を開始しました。関連した保健機能は免疫力増強、抗酸化、血脂低下及び睡眠改善に関わります。その後、大豆レシチン、クルクミン、果物と野菜のパウダーなどを含む17件の補助原料を健康食品届出製品に使用可能な補助原料リストに追加する公告も公布して、社会意見の募集を開始しました。
健康食品の届出制管理制度が施行した以来、国家市場監督管理総局が非「ビタミン・ミネラル補充」類健康食品届出製品に使用可能な原料に関する意見募集稿を公布するのは初めてです。中国の健康食品届出製品の原料目録は拡大され、市場活力が活発になり、企業の負担も軽減できると考えます。健康食品原料目録の拡大に伴い、未来に届出製品は健康食品の主要な傾向となると考えられます。
健康食品登録の審査認可速度の加速
「健康食品登録及び届出管理弁法」が施行した以来、健康食品登録製品の審査認可は一時停滞となります。2018年全年、認可された健康食品登録申請案は僅かな10件となります。健康食品登録の新旧政策交替及び中国国家機構の改革は主要な原因だと考えます。
2019年以来、健康食品登録製品の審査認可速度は顕著に加速しました。10月22日まで、認可された健康食品登録製品は668件あり、中に、新規製品登録の認可案は181件あり(詳しくは「2019年中国健康食品登録状況のまとめ」をクリックして確認してください)、期限延しの認可案は414件あり、登録情報変更の認可案は55件あり、技術移転の認可案は18件あります。詳細は下記の図表の通りです。
概して言えば、2018年に比べると、2019年中国健康食品登録製品の審査認可は穏やかに進行し、溜まられた件数は減少しています。今後、より多くの健康食品は登録認可が取得できると考えられます。
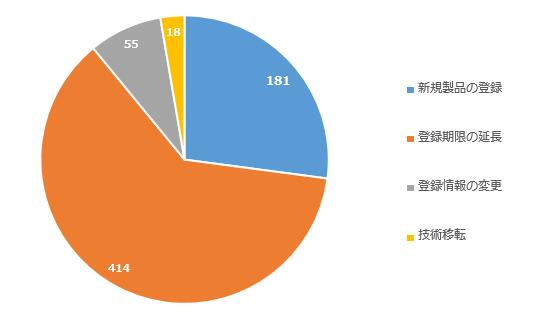
図1 2019年中国健康食品登録製品の認可件数
健康食品登録製品の検査方法の公表
「健康食品検験及び評価技術規範(2003版)」が2018年7月に廃止された後、健康食品を検験する根拠もなくなるため、新規製品登録の検験を一時停止した企業が多いです。
健康食品検験及び評価の管理を強化するために、国家市場監督管理総局は「健康食品検験及び評価技術規範」に対する修正を行いました。2019年、「健康食品毒理学評価プロセス」、「健康食品用菌種致病性評価プロセス」及び「健康食品衛生学理化検験規範」という3つの意見募集稿を公表しました。
機能評価方法の意見募集稿がまもなく公表されると見られます。目前、機能評価根拠がない問題を解決するために、「健康食品検験及び評価技術規範(2003版)」と2012年に修正された9つの保健機能評価方法は新バージョンに統合されて公布される見込みです。
いかなる単位および個人は原料目録又は機能目録に対して意見を提出可
「健康食品原料目録及び保健機能目録管理弁法」は2019年10月1日から施行されます。弁法に基づき、いかなる単位/個人は科学的な研究論証に基づいて保健機能原料目録及び保健機能目録に記載することに意見を提出することができます。政府機構は技術審査及び公開論証を行い、要求に合致したら目録に記載します。
これは全新的な法規制であり、健康食品管理に対して中国政府の開放的な態度を示し、企業の研究開発及び創新を励まし、社会資源を充分的に利用して科学的な研究を行うことを保証し、健康食品業界の発展を促進します。
まとめ
2019年以来、健康食品の新政策が相次いで公布し、製品を審査する効率を上げて、業界発展を支援しています。しかし、健康食品の応用及び販売に対する留意点もあります。健康食品登録製品に対して中国政府の技術審査は充分的な研究開発資料及び科学的根拠のサポートを重視するために、申請企業は製品の研究開発プロセス及び配合の科学的合理性を確保しなければなりません。
一方、企業の主体責任を強化し、消費者権利を保護するために、SAMRは健康食品のラベル管理(例えば、2020年1月1日以後、健康食品のラベルは警告用語及びクレームホットラインなどの情報を表示しなければならない)を強化し、虚偽宣伝を取り締まります。これも健康食品業界の発展に有利だと考えます。
お問い合わせ



