法規紹介
米国食品医薬品局(Food and Drug Administration、FDA)は、米国連邦保健・社会福祉省 (DHHS)傘下に設置する政府機構の1つであり、その職責は米国製造、或は米国向け輸出の食品(食品添加物も含む)、食品接触材料、医療機器、薬品などの安全を確保することです。これらの製品はFDAに登録申請や認証取得した後に、また米国市場に販売可能になります。
米国「連邦食品、薬品と化粧品法案」(FD&C 法案)に基づき、食品(食品添加物、健康食品なども含む)を製造、加工、包装、保存する企業(以下は「食品企業」と略称)は、FDA食品企業登録を完成しなければなりません。また、各偶数年の10月1日から12月31日までに登録を更新する必要で、しかも、「FD&C法案」許容範囲内のFDA工場視察を認めることを保証しなければなりません。
企業登録を完成する必要な食品類別
企業登録を完成する必要な食品類別 | 企業登録を完成する不要な食品類別 |
サプリメントとサプリメント成分(健康食品と健康食品原料) | 食品接触物質 |
乳幼児調製食品 | 殺虫剤 |
飲料(アルコール飲料と缶装水) | / |
果物と野菜 | / |
乳製品と卵殻 | / |
食品や食品成分としての初級農産物 | / |
缶装と冷凍食品 | / |
ベーキング食品、間食、キャンデー(チューインガムも含む) | / |
活き動物 | / |
動物食品(ペットフード、ペット間食と咀嚼物、動物飼料など) | / |
米国FDA食品企業登録の流れ
米国FDA食品企業登録を申請したい米国域外企業は、米国域内代理人を委託する必要で、しかも、登録申請する時に、企業を代表する唯一番号「ダンズナンバー(DUNS Number)」を提供しなければなりません。
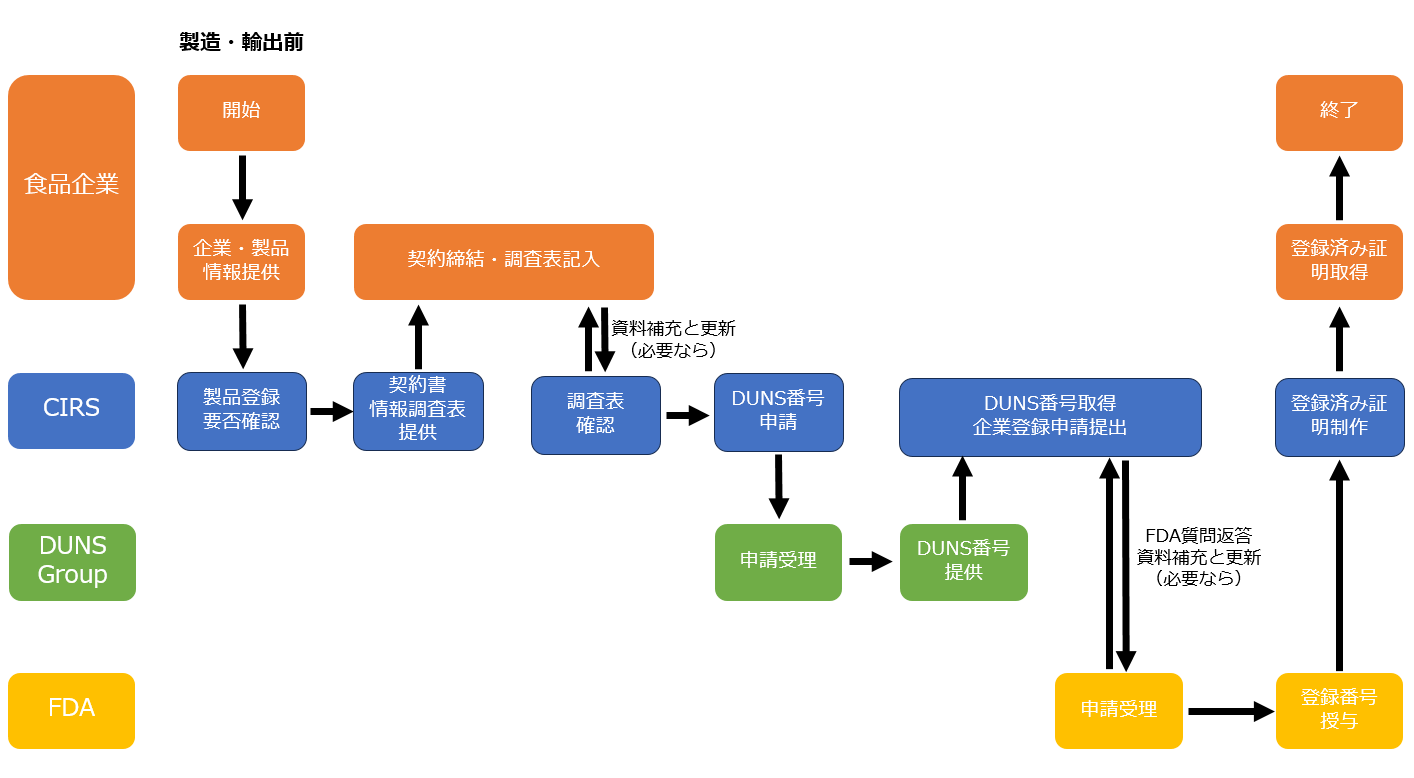
米国FDA食品企業登録の資料要求
- 企業名称、所在、電話番号
- DUNS番号
- 郵送宛先(企業所在と違うなら)
- 親会社名称、所在、電話番号(適用なら)
- 企業連絡者のメールアドレス(米国域外企業なら、米国代理人の名称、所在、電話番号、メールアドレス)
- 緊急連絡人の電話番号とメールアドレス
- 所有者、運営者、代理者の名称、所在、電話番号
- 企業の貿易名称
- 食品類別
- 各食品類別の相応する加工活動
- FDA工場視察認めの保証声明
- 資料真実性の保証声明
米国FDA食品企業登録についてよく聞かれる問題
Q:米国域外企業は、必ず米国域内代理人を委託する必要ですか。
A:そうです。米国FDA食品企業登録を申請する時、米国域外企業は、米国域内代理人を委託してFDAとのコミュニケーションを対応する必要です。
Q:米国当局は費用を請求しますか。
A:米国FDA食品企業登録を申請する時、米国当局は費用を請求しません。企業は代理機構に代理費用を支払えばいいです。
Q:所要時間はどのぐらいですか。
A:企業資料準備の所要時間に基づいて決定します。一般的に、2週間から1ヶ月間までの時間が必要です。
Q:登録完成後、何か証明書がありますか。
A:登録完成後、米国FDAは証明書を授与しません。ただし、登録完成後、企業はFDA登録番号(FDA Facility Registration No.)を取得でき、食品事前通告(Prior Notice)する時もこの登録番号を使用する必要です。CIRSは企業に証明書を交付し、CIRSを通して米国FDA食品企業登録を完成したことを証明します。
Q:登録は、有効期限がありますか。
A:登録完成後、有効期限はありません。ただし、各偶数年の10月1日から12月31日までに登録を更新しなければなりません。(強制的な要求)
Q:食品輸出の事前通告(Prior Notice)は何時に提出しますか。費用は必要ですか。
A: PNSIで提出する場合、事前通告は港到着日15日以内に提出する必要です。ABI/ACSで提出する場合、事前通告は港到着日30日以内に提出する必要です。食品輸出の事前通告は、輸出企業も輸入企業も提出でき、米国FDAは費用を請求しません。代理機構に依頼する場合、代理機構に代理費用を支払う必要です。
CIRSについて
CIRSは米国に完全子会社を有し、米国EPA及びFDAの相関認証に取り組み、豊富的な対応経験を持ちます。



