「中華人民共和国食品安全法」に基づき、新規食品添加物で食品を製造(既存食品添加物の使用範囲、使用量の拡大も含む)する場合、或は新規食品添加物を中国に輸入しようとする場合、企業は国務院衛生行政部門に関連した製品の安全性評価資料を提出しなければなりません。
中国において、新規食品添加物(中国では「食品添加剤」とも呼ぶ)として登録を要求される状況は以下通りです。
- 食品安全国家標準(GB)に収載されない新規食品添加物
- 国家衛生健康委員会の使用許可公告に収載されない食品添加物
- 使用範囲を拡大、或は使用量を拡大する食品添加物
新規食品添加物登録の関連法規
新規食品添加物登録の資料要求
1.申請書
2.通用名称、機能分類、使用量及び使用範囲
3.技術必要性及び使用効果の証明資料
4.品質規格要求、同添加物の使用方法及び検験方法、食品中同添加物の検験方法或は関連情況の説明
5.安全性評価報告 製造原材料或は供給源、化学構成及び物理特性、製造工芸、毒理学安全性評価資料或は検験報告、品質規格検験報告
6.ラベル或は説明書の見本
7.他の国家(地域)、国際組織によって製造及び使用許可証明などの安全性評価に役立つ資料
8.委託書(申請を委託する場合、提供必要)
既存食品添加物の使用量拡大及び使用範囲拡大を申請する場合、安全性評価報告の提出は不要です。
輸入新規食品添加物の初回登録を申請する場合、以下の資料を追加提出しなければなりません。
9.輸出国(地域)所管部門或は機構によって発行された同国(地域)における製造/販売の証明書類
10.製造企業所在国(地域)の所管機構又は組織によって製造企業の審査又は認証の証明書類
新規食品添加物登録の試験要求
種類 | 必要な試験 |
品質規格試験報告 | 申請資料に記載された品質規格要求及び検験方法に従い、3ロットの食品添加物を試験する |
安全性評価報告 | 「GB 15193.1-2014 食品安全国家標準 食品安全性毒理学評価プロセス」に従って試験を行う 或は同物質に対して外国GLP実験室によって出した毒理学評価報告資料を提供する |
新規食品添加物登録の流れ
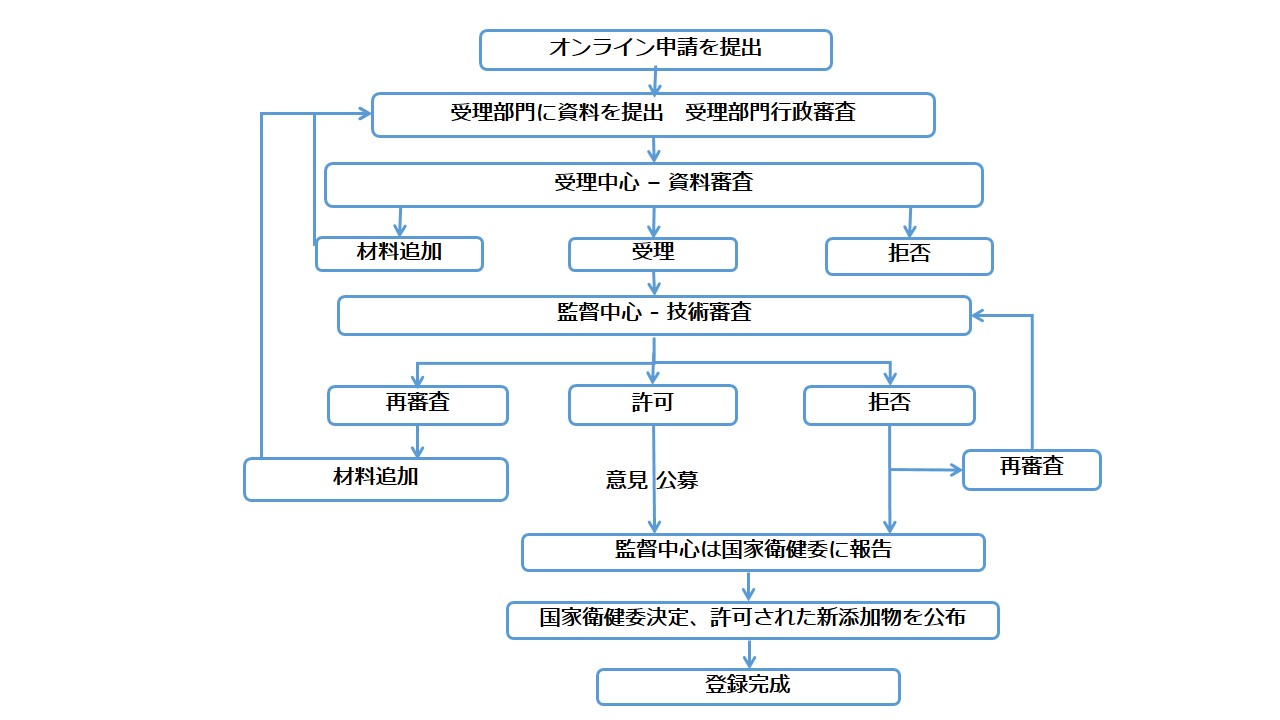
CIRSのサービス
• 新規食品添加物の法規トレーニング
• 新規食品添加物の法規動向モニタリング
• 新規食品添加物登録の代行
• 単項目技術サービス
√ 登録実行性分析
√ 資料ギャップ分析
√ 書類準備
√ 翻訳及び公証
√ 試験手配及び進捗フォローアップ
√ 技術審査答弁



