2020年6月29日に「化粧品監督管理条例」(国令第727号)が発表されて以来、一連の関連法規が相次いで発表され、その中に化粧品新原料の登録備案に関連する新法規文書には「化粧品登録備案管理弁法」、「化粧品新原料登録備案資料管理規定」及び「化粧品安全評価技術ガイドライン」などが含まれています。2021年5月1日から、化粧品新原料登録備案はGMPAオンライン事務ホールの化粧品スマート申告審査評価システムで申請する必要があります。新法規が施行されて以来、2021年5月1日から2022年6月28日までの間に、計18の化粧品新原料が備案を成功しました。その中、13件は国産化粧品新原料、5件は輸入化粧品新原料に属します。
表1 新法規の下で備案完了の国産化粧品新原料情報
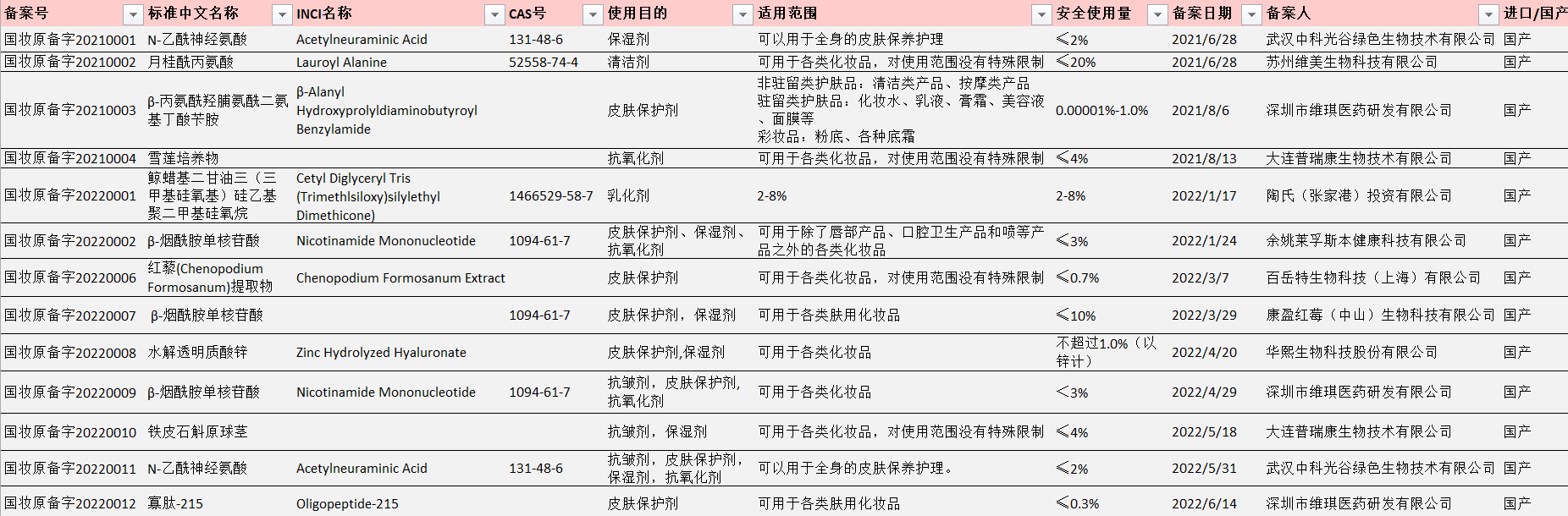
データの出典:GMPA公式サイト
表2 新法規の下で備案完了の輸入化粧品新原料情報

データの出典:GMPA公式サイト
旧法規「化粧品衛生監督管理条例」の下で、2004年から2021年5月1日までに14の新原料が承認されました(具体的な情報は表3を参照)。
表3 2004-2021年5月1日までに承認された化粧品新原料
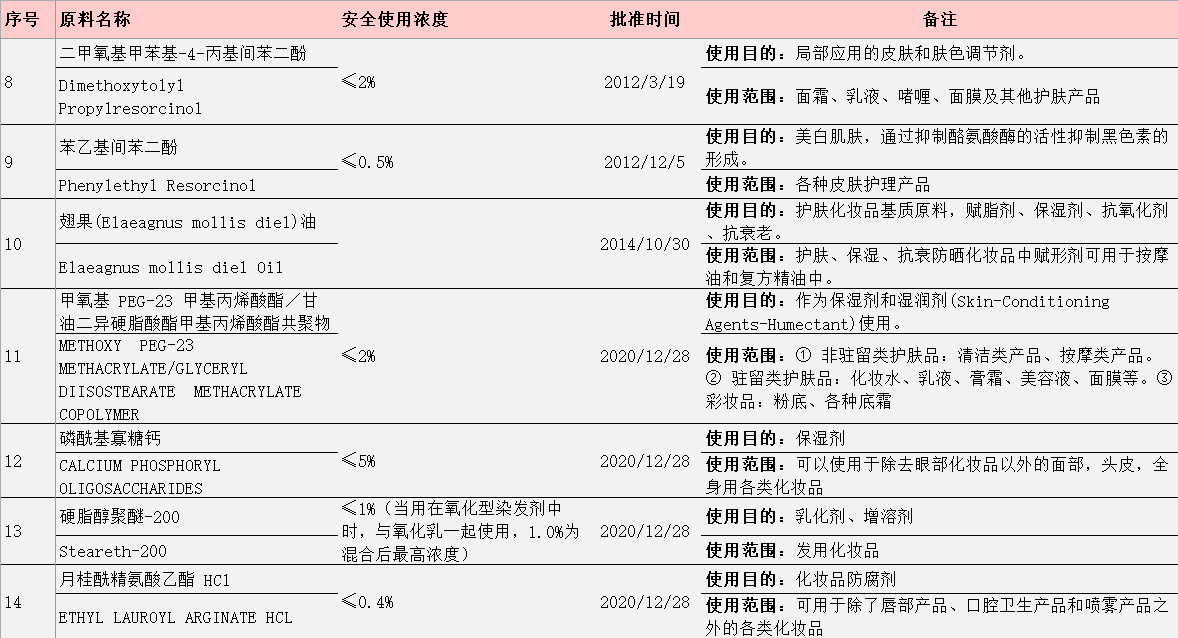
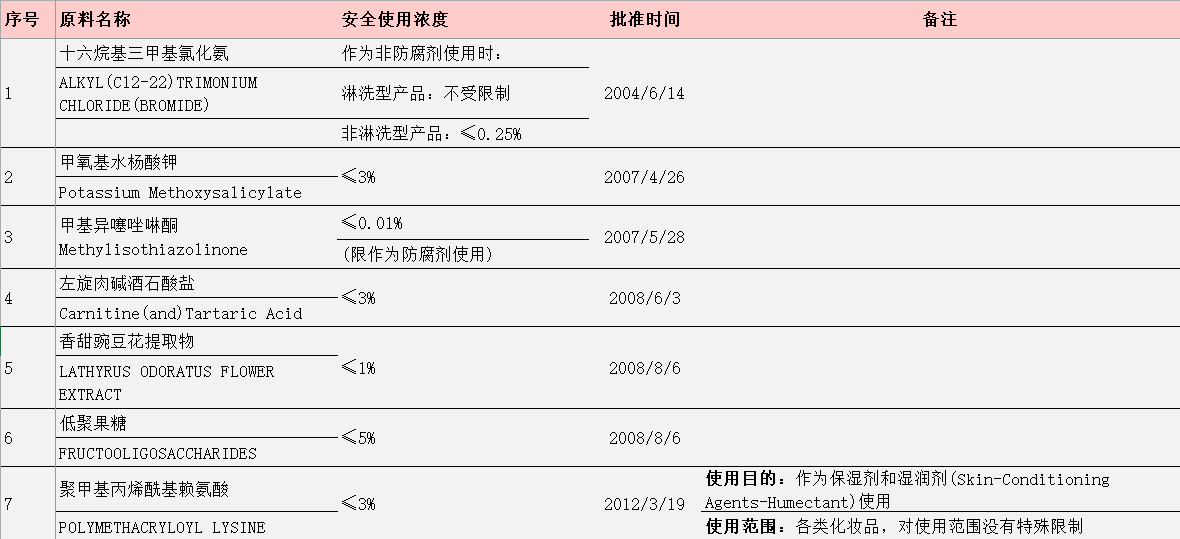
データの出典:主管部門の公式サイト
上表中の原料1-6号は元衛生部に承認され、原料7-10号は元国家食品薬品監督管理(総)局に承認され、11-14号はGMPAに承認されました。これらの原料の審査プロセスから、関係する国家機関の変遷と交代が見えます。2008年9月に化粧品の衛生行政許可は衛生部から国家食品薬品監督管理局に移管されました。2013年3月22日、国家食品薬品監督管理局(State Food and Drug Administration、略称SFDA)は国家食品薬品監督管理総局(China Food and Drug Administration、略称CFDA)に改称しました。2018年4月10日、国務院機構の改革において、「国家食品薬品監督管理総局」も正式に「国家薬品監督管理局」に変更されました。
CIRS Groupの化粧品コンプライアンスプラットフォーム(妆合规)の中国化粧品原料法規データベースには、新旧法規の下で登録備案された化粧品の新原料リストを収録しており、企業の日常的な配合の研究開発と製品コンプライアンス業務の展開を支援し、研究開発コンプライアンスのコストとリスクを低減させます。



