米国GRAS認証紹介
「GRAS」は「Generally Recognized As Safe(一般に安全とみなされている)」の略語であり、米国食品医薬品局(FDA)より与えられる安全基準合格証です。
GRAS認証の国際認可度は高くて、食品原料または食品添加物の国際市場進入の重要通行証とも言えます。
米国GRAS認証の主要内容
GRAS認証の分類
米国GRAS認証は「GRAS自己声明(Self-affirmed GRAS)」及び「FDA GRAS認証(FDA GRAS Notice)」という2種類に分けられます。
① GRAS自己声明(Self-affirmed GRAS)
専門家より物質安全性への認可です。GRAS自己声明は、米国FDAに提出しなくて、米国FDAの審査を通過不要です。一般的に、公開しません。
② FDA GRAS認証(FDA GRAS Notice)
米国FDAに正式提出し、米国FDAの審査を通過する必要です。米国FDAの結論は「異議なし(FDA has no questions)」であれば、GRASリストに収載され、米国FDA公式サイトにて検索できます。米国FDAの認可を取得したので、この類別のGRASの権威性は更に高くて、更に認可されます。
GRAS認証の申請者
いかなる個人や機構は、米国FDAにGRAS認証を申請できます。
GRAS認証の一般流れ
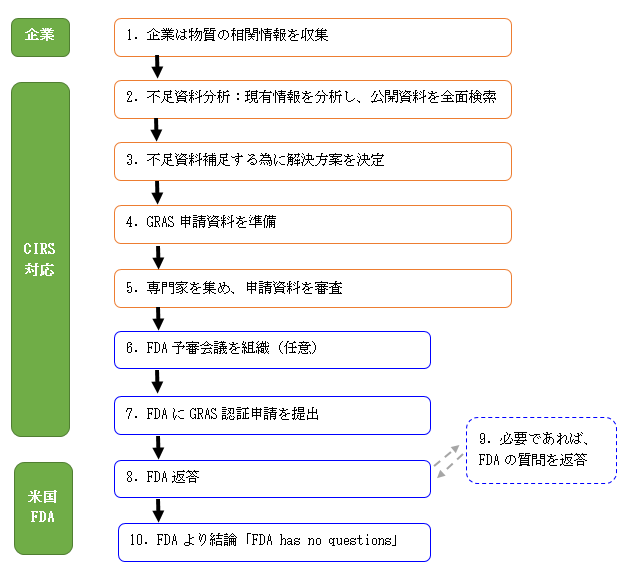
注:ステップ1-5は「GRAS自己声明」の一般流れです。そして、「FDA GRAS認証」ならステップ6-10を追加して進行する。
GRAS認証の一般資料要求
一般的に、不足資料を分析する為に、企業は以下の資料を提出する必要です。
- 物質の基礎情報。例えば、物質の定義、通用名称、化学名称、商品名称、化学構造、相対分子重量、など。
- 物質が食品への予期用途と使用量。
- 製造工程。
- 品質規格および関連した分析報告。
- 食品自己限定性のレベル。
- 食品への使用歴史。
- 安全性論述。
GRAS認証の推定周期
主要ステップ | 推定周期 |
不足資料分析 | 1ヶ月 |
GRAS申請資料の準備と提出 | 3-6ヶ月 |
FDA審査 | 6ヶ月(特殊状況であれば、9ヶ月までに延ばす) |
総計 | 10-16ヶ月 |
CIRSのサービス
- 米国 GRAS自己声明
- 米国 FDA GRAS認証
- 中国 新食品原料登録
- 中国 新規食品添加物登録
- 中国 遺伝子組み換え微生物に関わる新規食品添加物登録



